京都电子KEM中国 官方产品咨询电话:021-54488867、400-820-2557 咨询邮箱:kemu-kem@163.com

 范围、产品分类和术语定义
范围、产品分类和术语定义
本文件给出了脂肪酶制剂的产品分类,规定了技术要求、检验规则、标志、包装、运输和贮存,并描述了相应的试验方法。
本文件适用于微生物发酵生产的脂肪酶制剂产品的生产、检验和销售。
下列术语和定义适用于本文件。
脂肪酶 lipase
能水解甘油三酯(含天然油脂)或脂肪酸酯产生单或双甘油酯或甘油和游离脂肪酸,在特定条件下也能催化酯合成和酯交换反应的酶。
脂肪酶制剂 lipase preparations
以脂肪酶为主要催化活性组分,通过制剂等工艺制得的产品。
注:制剂工艺中能加入有助于产品贮存、稳定和使用的辅料。
脂肪酶活力 lipase activity
脂肪酶制剂的酶活力 activity of lipase preparations
1g固体脂肪酶制剂(或1mL液体脂肪酶制剂)含有的酶活力单位。
注1:以U/g(或U/mL)表示。
注2:在一定温度和pH条件下,脂肪酶每分钟水解底物产生1μmol的可滴定的脂肪酸,即为脂肪酶1个酶活力单位(以U表示)。也能根据所采用的酶活力测定方法,另行约定相应的酶活力单位。
产品分类
按产品的应用领域
食品工业用和其他工业用脂肪酶制剂。
按产品的形态
固体剂型(含粉末剂型、颗粒剂型和固定化剂型)和液体剂型脂肪酶制剂。 要求
要求
感官要求
应符合表1的规定。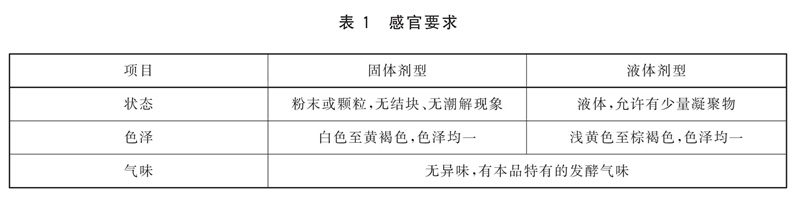
理化要求
应符合表2的规定。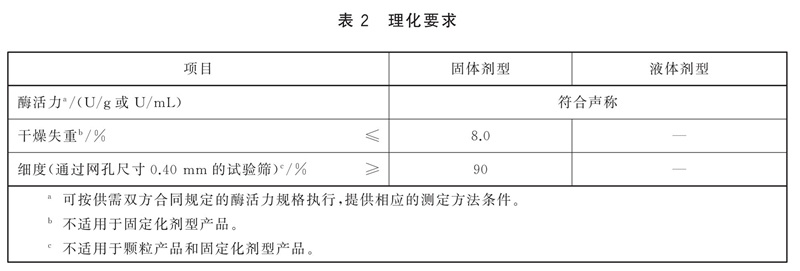
 试验方法
试验方法
酶活力
根据底物适应性,测定水解橄榄油底物的酶活力时,按附录A进行检测;测定水解三丁酸甘油酯底物的酶活力时,可参考附录B。也可根据实际需求采用其他方法进行检测。
附录A (规范性)
脂肪酶制剂活力的测定滴定法
A.1 原理
脂肪酶在一定条件下,能使甘油三酯水解成脂肪酸、甘油二酯、甘油单酯和甘油,所释放的脂肪酸可用标准碱溶液进行中和滴定,用pH计指示反应终点,根据消耗的碱量,计算其酶活力。
反应式为:![]()
A.2 试剂和材料
A.2.1 聚乙烯醇:聚合度1750±50。
A.2.2 橄榄油:试验试剂。
A.2.3 无水乙醇。
A.2.4 磷酸二氢钾。
A.2.5 十二水磷酸氢二钠。
A.2.6 氢氧化钠。
A.3 溶液配制
A.3.1 聚乙烯醇溶液(4%):称取聚乙烯醇40g(精确至0.1g),加水800mL,在沸水浴中加热,搅拌,直至全部溶解,冷却定容至1000mL。
注:根据乳化效果和溶解情况,也能选择使用2%的聚乙烯醇溶液。
A.3.2 底物溶液:称量聚乙烯醇溶液150g, 加橄榄油50g,用高速匀浆机10000r/min处理6min(分2次处理,间隔5min,每次处理3min),水浴控制温度,处理过程中温度维持在60°C,处理结束后常温下磁力搅拌20min。底物溶液显微镜观察应有80%以上的液滴直径小于或等于3μm。该溶液现配现用。
注:也能选其他转速,并根据乳化效果延长或缩短均质时间。
A.3.3 磷酸缓冲溶液(pH=7.5):分别称取磷酸二氢钾1.96g和十二水磷酸氢二钠39.62g,用水溶解并定容至500mL。如需要,调节溶液的pH至7.5±0.05。
A.3.4 氢氧化钠标准溶液[c(NaOH)=0.05mol/L上按 GB/T 601 的规定配制与标定0.5mol/L氢氧化钠标准滴定溶液。使用时,准确稀释10倍。
注:也能采用商品化的氢氧化钠标准溶液。
A.3.5 乙醇溶液(95%,体积分数)。
A.3.6 酚酞指示液(10g/L):按 GB/T 603 的规定配制。
A.4 仪器和设备
A.4.1 磁力搅拌水浴锅:±0.2°C。
A.4.2 电子天平:感量0.1mg。
A.4.3 移液器。
A.4.4 酸度计:精度±0.01。
A.4.5 秒表。
A.4.6 高速匀浆机。
A.4.7 电位滴定仪。
A.4.8 光学显微镜。
A.4.9 微量滴定管:10mL,分刻度≤0.05mL。
A.5 分析步骤
A.5.1 样品前处理
称取酶样品1.00g(精确至0.1mg)或1.0mL,加入适量磷酸缓冲溶液磁力搅拌溶解15min并稀释,稀释酶液采用玻璃器皿,测定时控制酶液浓度,样品与对照消耗碱量之差控制在1.0mL~2.0mL范围内,吸取样品时,应将酶液摇匀后再取。
注:酶会附着在塑料上,因此用玻璃器皿溶解稀释和滴定。使用塑料枪头短时间转移的情况除外。
A.5.2 测定
A.5.2.1 电位滴定法(仲裁法)
按电位滴定仪使用说明书对仪器进行校正(若使用酸度计进行试验, 则按照酸度计说明书对酸度计进行校正)。
取4个100mL烧杯,于空白杯(A)和样品杯(B1、B2、B3)中各加入4.0mL底物溶液,5.0mL磷酸缓冲溶液,再于A杯中加入15.00mL 95%乙醇溶液。40°C±0.2°C水浴中磁力搅拌预热5min,然后于空白杯(A)和样品杯(B1、B2、B3)中各加1.00mL待测酶液,准确反应15min后,于样品杯(B1、B2、B3)中立即补加15.00mL 95%乙醇溶液终止反应。
在每个烧杯中加25mL蒸馏水,置于电位滴定仪上(若使用酸度计,则将酸度计电极放入烧杯中),边搅拌,边用氢氧化钠标准溶液滴定,直至pH10.3为滴定终点,记录消耗氢氧化钠标准溶液的体积。
注:对于某些脂肪酶样品加入25mL蒸馏水影响酶活检测结果,此类样品在终止反应后直接进行氢氧化钠标准溶液滴定。
日本京都电子KEM适配仪器,一键点击直达:
京都电子KEM 电位滴定仪&动态滴定(pH-stat)功能的滴定仪 AT-710S
自动电位滴定仪操作视频:
A.5.2.2 指示剂滴定法
取2个100mL锥形瓶,分别于空白瓶(A)和样品瓶(B)中各加入底物溶液4.00mL和磷酸缓冲液5.00mL,再于A瓶中加入95%乙醇溶液15.00mL,于40°C±0.2°C水浴中预热5min,然后于空白瓶(A)、样品瓶(B)中各加待测酶液1.00mL,立即混匀计时,准确反应15min后,于样品瓶(B)中立即补加95%乙醇溶液15.0mL终止反应,取出。
于空白和样品溶液中各加酚酞指示液两滴,用氢氧化钠标准溶液滴定,直至微红色并保持30s不褪色为滴定终点,记录消耗氢氧化钠标准溶液的体积。
A.6 计算
脂肪酶制剂的酶活力按公式(A .1)计算:![]()
式中:
X1——样品的酶活力,单位为酶活力单位每克或酶活力单位每毫升(U/g或U/mL);
V1——滴定样品溶液时消耗氢氧化钠标准溶液的体积,单位为毫升(mL);
V2——滴定空白溶液时消耗氢氧化钠标准溶液的体积,单位为毫升(mL);
c ——氢氧化钠标准溶液浓度,单位为摩尔每升(mol/L);
50——0.05mol/L氢氧化钠溶液1.00mL相当于脂肪酸50μmol;
n1——样品的稀释倍数;
0.05——氢氧化钠标准溶液浓度换算系数;
15——反应时间15min。
A.7 结果表示
所得结果表示至整数。
A.8 精密度
在重复性条件下获得的两次独立测定结果的绝对差值应不超过算术平均值的10%。
附录B (资料性)
脂肪酶制剂活力的测定动态滴定法
B.1 方法信息
B.1.1 原理
脂肪酶水解甘油三酯生成脂肪酸,使反应体系的pH下降。通过连续加入碱的方法保持反应体系的pH恒定。碱滴定的速率与酶活力成比例。酯酶的存在会使检测的脂肪酶的活力增加。蛋白酶的存在降解脂肪酶,从而使检测到的脂肪酶的活力减小。
注:洗涤剂的存在会严重影响本方法。依不同洗涤剂的类型和浓度不同,这种影响表现为从完全抑制到激活。酶会附着在塑料上,因此用玻璃器皿溶解稀释和滴定,使用塑料枪头短时间转移的情况除外。
B.1.2 反应式
反应式为: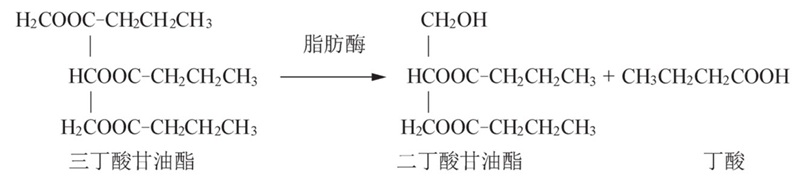
B.1.3 反应条件
反应条件如下:
——温度:30°C±1°C;
——pH:7.00;
——底物浓度:0.16mol/L的三丁酸甘油酯;
——反应时间:至少1.5min(只有线性反应区用于计算斜率)。
B.1.4 分析范围
样品的分析范围为0.2U/mL~4.0U/mL。如果可能,所有样品在1.5U/mL~4.0U/mL的范围内被分析。
B.1.5 检测限
对于液体样品,检测限为20U/g,相当于2.5g样品溶解在10mL溶液中,然后再稀释25倍。对于固体样品,检测限为50U/g,相当于1.0g样品溶解在10mL溶液中,然后再稀释25倍。
B.2 仪器和设备
B.2.1 动态滴定(pH-stat)功能的滴定仪。
B.2.2 乳化器。
B.2.3 恒温水浴:精度±0.2°C。
B.2.4 温度计:精度±0.2°C。
B.2.5 自动移液器。
B.3 试剂
除非另有说明,在分析中仅使用确认为分析纯的试剂和蒸馏水或去离子水或相当纯度的水。
B.3.1 三丁酸甘油酯(C15H26O6)。
B.3.2 氯化钠(NaCl)。
B.3.3 磷酸二氢钾(KH2PO4)。
B.3.4 阿拉伯胶。
B.3.5 甘氨酸(H2NCH2COOH)。
B.3.6 甘油[HOCH2CHCOH)CH2OH]。
B.3.7 氢氧化钠片剂(NaOH)。
B.3.8 电极校正液(pH7.0)。
B.3.9 电极校正液(pH4.01)。
B.3.10 乙醇溶液(96%,体积分数)。
B.3.11 氮气(N2)。
B.3.12 氢氧化钠溶液[c(NaOH)=1mol/L]:按照 GB/T 601 的规定配制。
B.3.13 氢氧化钠滴定液[c(NaOH)=0.025mol/L]:取氢氧化钠溶液25mL,用水稀释并定容至1000mL。配好后需用适宜的设备脱气。
B.3.14 氢氧化钠滴定液[c(NaOH)=0.005mol/L上取氢氧化钠滴定液25mL,用水稀释并定容至5000mL。
B.3.15 乳化剂:移取约180mL去离子水于500mL烧杯中,加入搅拌子高速搅拌,再缓慢加入30.0g阿拉伯胶,继续搅拌至全部溶解。另取500mL烧杯,加入53.7g氯化钠和1.20g磷酸二氢钾,再加入350mL水充分溶解。将1620mL甘油置于3L容量瓶中,再依次加入上述氯化钠-磷酸二氢钾溶液和阿拉伯胶溶液,最后以水定容并混匀。
B.3.16 底物乳剂:称取三丁酸甘油酯62.5g,分别量取乳化剂200mL和水940mL,混合。将混合液用匀浆器处理3min(7000r/min)。匀浆后的溶液先用普通的磁力搅拌器搅拌至少20min,然后调节pH至4.75±0.05。
注:不同来源和批号的三丁酸甘油酯和阿拉伯胶对试验结果有影响,在更换产品或批号前需进行有效性确认。
B.3.17 甘氨酸缓冲液1(7.51g/L):称取甘氨酸37.54g和氢氧化钠片剂18.5g,用水溶解并定容至5L。如需要,调节溶液的pH至10.8±0.05。
B.3.18 甘氨酸缓冲液2(0.75g/L):取100mL甘氨酸缓冲液1,用水定容至1000mL。如需要,调节溶液的pH至10.8±0.05。
B.4 标准曲线和样品处理
B.4.1 标准曲线
称取一定量的已知活力酶标准品,精确至0.0001g,用甘氨酸缓冲液2溶解并稀释,制成标准储备液。标准储备液的浓度为20U/mL。然后按照表B.1配制溶液,并绘制标准曲线。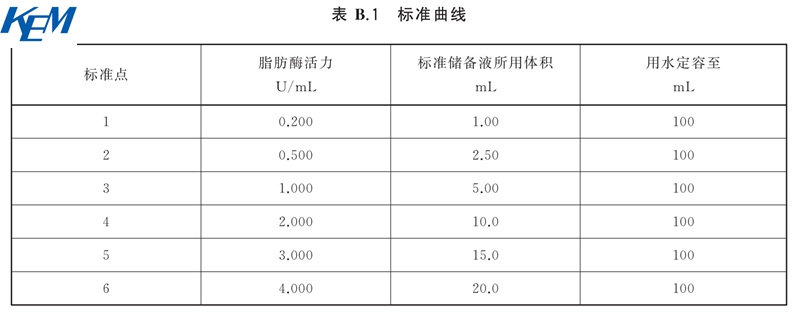
B.4.2 标准对照
可使用已知活力的样品作为标准对照。标准对照的处理同样品。
B.4.3 样品处理
不同的样品需做不同的预处理,以激活或保护在样品基质中的脂肪酶。
可考虑采用甘氨酸缓冲液1和水来分别溶解和稀释样品的方法,或采用甘氨酸缓冲液2来溶解和稀释样品的方法,或直接用水溶解和稀释样品的方法,以求得到最好的效果。样品的溶解液和稀释液需搅拌均匀。样品最终稀释到酶活力在1.5U/mL~ 4.0U/mL范围内。如可能,样品稀释完立即测定。
B.5 分析步骤
B.5.1 系统准备
B.5.1.1 按照无水乙醇、适当的肥皂水、热水、去离子水、底物的顺序清洗滴定容器和管路。保证水浴的温度在30.0°C±0.5°C。
B.5.1.2 校正pH电极:使用前需校正pH电极的灵敏度在95%~102%;pH7.00在6.985~6.989之间;pH4.01在4.009~4.012之间。如果达不到此标准,按照pH电极使用说明进行冲洗并再次校正。
B.5.2 分析
B.5.2.1 pH 电极用后浸泡在饱和的氯化钾(KCl)溶液中,使用前冲洗。在反应溶液表面用氮气吹充,以防止空气中二氧化碳的干扰。分析前一定要保证底物的温度为30.0°C±0.5°C。在分析每个样品前要用0.005mol/L的氢氧化钠滴定液冲洗滴定皿和管路。
B.5.2.2 试验步骤如下。
——将15mL的底物加入滴定皿中。滴定前pH电极的读数应小于7.0。
——加1mL样品稀释液加入滴定皿中。反应体系的pH在滴定过程中保持在7.0。记录为保持恒定pH而加入的滴定液的量。
——滴定结束后滴定仪打印出滴定曲线线性范围的平均斜率(如果使用不同的设备,数据可能以其他形式输出)。滴定曲线需有一段持续1.5min的线性输出。
——先分析标准曲线(每个标准点分析一次),再分析一个标准对照,最后分析样品(每个样品分析一次)。需注意, 一天内非一次运行的样品不能使用相同的标准曲线。如果样品在当天晚些时候分析,标准溶液要重新分析。
——每个样品分析前和最后一个样品完成分析后,系统将进行冲洗。排空底物容器和管路,并用乙醇冲洗。如果系统将在一周以上时间不再使用,则需用去离子水进行冲洗并用氢氧化钠滴定液或相同浓度的盐酸溶液充满敏感部件,避免出现盐类结晶。
B.6 计算
B.6.1 结果计算
利用标准点的测定值作标准曲线,其中X轴为标准品酶活力,Y轴为相应的滴定反应的平均斜率(mL/min)。标准曲线为一条直线。样品稀释液的活力从标准曲线中读出,然后按公式(B.1)计算:![]()
式中:
X2——样品的酶活力,单位为酶活力单位每克(U/g)或酶活力单位每毫升(U/mL);
A ——稀释样品在标准曲线上读出的酶活力,单位为酶活力单位每毫升(U/mL);
V3——样品溶解用的容量瓶体积,单位为毫升(mL);
n2——第二次稀释的倍数;
m3——样品的质量或体积,单位为克(g)或毫升(mL)。
B.6.2 结果的确认
当满足以下条件时可以确认本次分析有效。
a) 标准对照的检测值在本方法所规定的可接受偏差范围内。
b) 标准曲线的斜率满足:
1) 标准点1小于0.02mL/min;
2) 标准点6在0.14mL/min~0.18mL/min之间。
c) 标准曲线的相关系数(r2)大于或等于0.995。
d) 标准点3~点6相关系数(r2)大于0.9995。标准点1~点2的r2大于0.995是可接受的。如果达不到此条件,检查分析系统。
B.6.3 结果的表示
结果给出3位有效数字。如果结果低于检测限,则表示为小于20U/g(液体)或小于50U/g(固体)。
B.7 精密度
在重复性条件下获得的两次独立测定结果的绝对差值应不超过算术平均值的5%。
可睦电子 KEM CHINA
电话:400-820-2557 邮编:200030 传真:021-54480010 公司地址:上海市徐汇区宜山路333号汇鑫国际大厦1201室
Copyright(C) 2012–2023 可睦电子(上海)商贸有限公司 沪ICP备10207403号-1 沪公网安备31010402002220号 沪(徐)应急管危经许[2022]203762
本网站尚在建设中,部分资料有所缺失,若有不便,敬请谅解!